研究者利用DART-seq技术,通过APOBEC1-YTH融合蛋白在活细胞中诱导m6A位点附近的C-to-U突变,以实现单核苷酸分辨率的m6A识别。研究发现,这些C-to-U突变并非集中于m6A邻近位置,而倾向于在距离m6A位点100 nt范围内聚集成簇。那么这些距离在10100nt范围内的突变能够用于标记m6A位点,而不会干扰ONT DRS中m6A甲基化5-mer的电流信号。基于这种内源性标记策略,研究团队利用在ONT DRS数据中提取了1,020,237个读长水平的5-mer m6A信号,并结合深度残差神经网络,成功开发了能够在单条读长水平上识别m6A的工具m6Aiso。此外,研究者还采用了kaiyun欧洲杯的SURFSeq 5000平台完成了A549细胞系的GLORI测序,为m6Aiso 在多个细胞系中的准确性评估提供了有力的支撑,同时也反映了SURFSeq 5000平台进行二代高通量测序具有高度的可靠性。如下图所示,研究团队在多个细胞系中比较了m6Aiso以及GLORI测序得到的m6A修饰水平,m6Aiso在HEK293T, HeLa, A549, mESC中都和GLORI高度一致,其中HEK293T, HeLa和 mESC的GLORI数据来源于原始的GLORI论文,而A549细胞的GLORI数据为团队自行建库后采用SURFSeq 5000平台完成的测序。
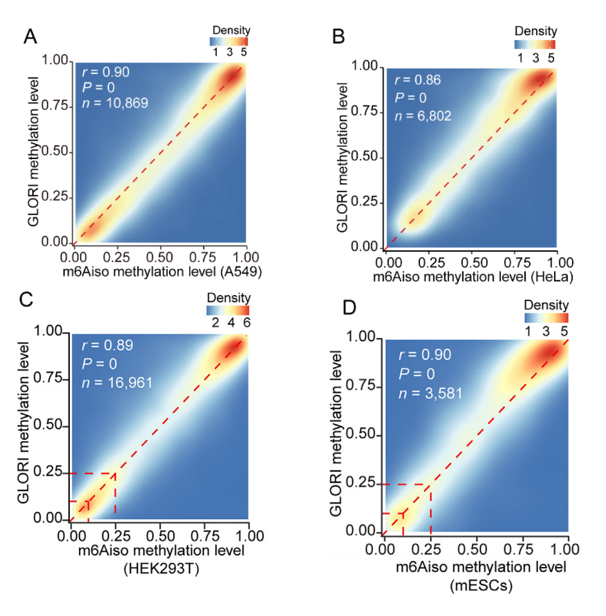
图1 不同细胞系m6Aiso和GLORI测序得到的m6A修饰水平比较
利用工具m6Aiso,研究者阐述了相同m6A位点不同的异构体上形成差异化m6A修饰的三种机制:1、EJC(外显子连接复合体)对m6A抑制的差异,与之前的研究一致,发现EJC会抑制靠近外显子边界的m6A沉积,即在异构体中外显子边界200 bp范围内的m6A甲基化水平较低;2、RNA结合蛋白对不同异构体RNA的特异性结合,如TARBP2结合内含子的邻近外显子上的m6A位点的甲基化水平显著高于未结合TARBP2内含子的邻近外显子;3、转录因子也会调控m6A,主要通过共转录的方式招募m6A 的甲基化转移酶来修饰其转录的RNA,因此使用不同启动子的RNA由于转录因子不同而产生差异的m6A修饰。由于变化的m6A位点位于共同的3'UTR,而短读长测序无法确定每个亚型的具体5'区域,因此这一发现进一步强调了在研究m6A动态变化时使用长读长测序的必要性。
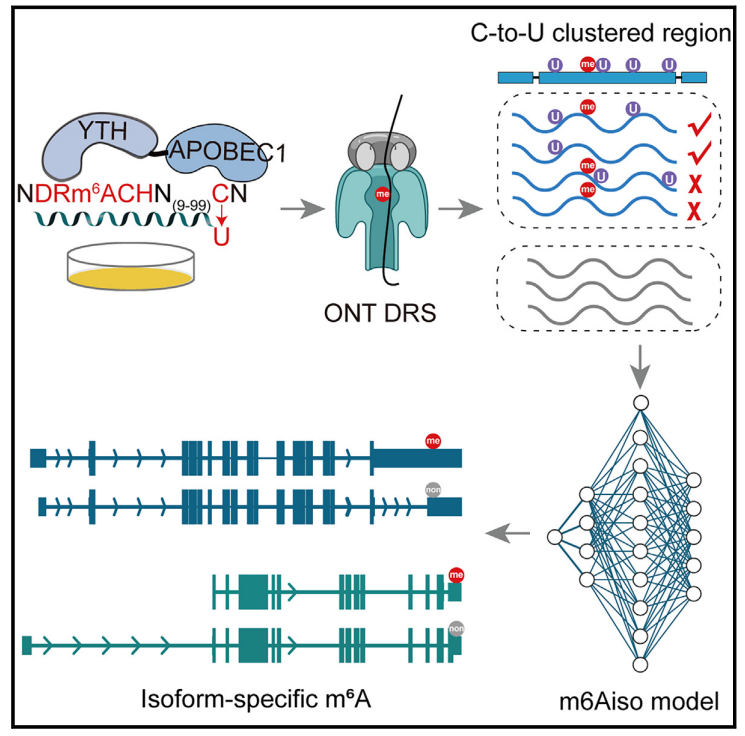
图2 m6A在单reads上的内源性标记和m6Aiso在单分子水平上的结果评价